Cara bateri berfungsi dan berfungsi
 Dalam erti kata yang paling luas dalam teknologi, istilah "bateri" merujuk kepada peranti yang membenarkan dalam keadaan operasi tertentu untuk mengumpul jenis tenaga tertentu, dan pada orang lain menggunakannya untuk keperluan manusia.
Dalam erti kata yang paling luas dalam teknologi, istilah "bateri" merujuk kepada peranti yang membenarkan dalam keadaan operasi tertentu untuk mengumpul jenis tenaga tertentu, dan pada orang lain menggunakannya untuk keperluan manusia.
Ia digunakan di mana ia perlu untuk mengumpul tenaga untuk masa tertentu dan kemudian menggunakannya untuk menjalankan proses intensif buruh yang besar. Sebagai contoh, akumulator hidraulik yang digunakan dalam kunci membolehkan kapal naik ke tahap baharu di dasar sungai.
Bateri elektrik berfungsi dengan elektrik pada prinsip yang sama: pertama, ia mengumpul (mengumpul) elektrik daripada sumber pengecasan luaran dan kemudian memberikannya kepada pengguna yang bersambung untuk melakukan kerja. Mengikut sifatnya, ia tergolong dalam sumber arus kimia yang mampu menjalankan kitaran berkala nyahcas dan mengecas berulang kali.
Semasa operasi, tindak balas kimia sentiasa berlaku di antara komponen plat elektrod dengan bahan pengisinya - elektrolit.
Gambarajah skematik peranti bateri boleh diwakili dengan lukisan dipermudahkan apabila dua plat logam berbeza dengan wayar dimasukkan ke dalam badan vesel untuk menyediakan sesentuh elektrik. Elektrolit dituangkan di antara plat.
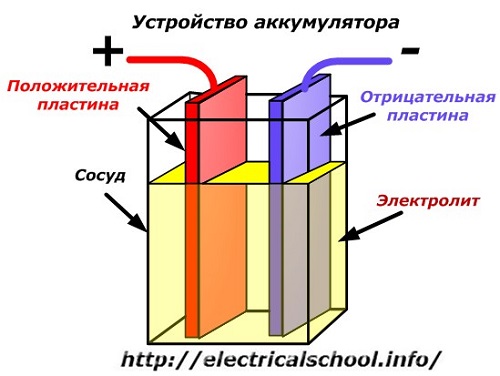
Operasi bateri apabila dinyahcas
Apabila beban, seperti mentol lampu, disambungkan ke elektrod, litar elektrik tertutup dicipta yang melaluinya arus nyahcas mengalir. Ia dibentuk oleh pergerakan elektron dalam bahagian logam dan anion dengan kation dalam elektrolit.
Proses ini secara konvensional ditunjukkan pada rajah dengan reka bentuk elektrod nikel-kadmium.
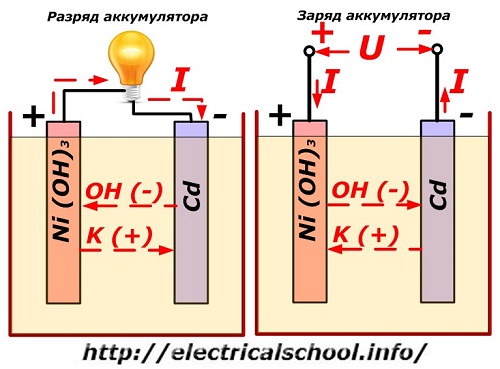
Di sini, oksida nikel dengan bahan tambahan grafit, yang meningkatkan kekonduksian elektrik, digunakan sebagai bahan elektrod positif. Logam elektrod negatif ialah kadmium span.
Semasa pelepasan, zarah oksigen aktif daripada nikel oksida dilepaskan ke dalam elektrolit dan diarahkan ke plat negatif, di mana kadmium teroksida.
Prestasi bateri semasa mengecas
Apabila beban dimatikan, voltan malar (dalam situasi tertentu, berdenyut) digunakan pada terminal plat dengan nilai yang lebih besar daripada bateri yang dicas dengan polariti yang sama, apabila terminal tambah dan tolak sumber dan pengguna bertepatan .
Pengecas sentiasa mempunyai lebih kuasa, yang "menindas" sisa tenaga dalam bateri dan mencipta arus elektrik dalam arah yang bertentangan dengan pelepasan. Akibatnya, proses kimia dalaman antara elektrod dan elektrolit berubah. Sebagai contoh, pada kotak plat nikel-kadmium, elektrod positif diperkaya dengan oksigen, dan negatif - kepada keadaan kadmium tulen.
Apabila bateri dinyahcas dan dicas, komposisi kimia bahan plat (elektrod) berubah, tetapi elektrolit tidak berubah.
Kaedah sambungan bateri
Sambungan selari
Jumlah arus nyahcas seseorang boleh tahan bergantung pada banyak faktor, tetapi terutamanya reka bentuk, bahan yang digunakan dan dimensinya. Lebih besar kawasan plat pada elektrod, lebih besar arus yang boleh ditahan.
Prinsip ini digunakan untuk menyambungkan sel-sel jenis yang sama secara selari dalam bateri apabila perlu untuk meningkatkan arus ke beban.Tetapi untuk mengecas reka bentuk sedemikian, adalah perlu untuk meningkatkan kuasa sumber. Kaedah ini jarang digunakan untuk struktur siap pakai, kerana kini lebih mudah untuk segera membeli bateri yang diperlukan. Tetapi pengeluar bateri asid menggunakannya, menyambungkan plat berbeza ke dalam blok tunggal.
Sambungan bersiri
Bergantung pada bahan yang digunakan, voltan 1.2 / 1.5 atau 2.0 volt boleh dijana antara dua plat elektrod bateri yang biasa dalam kehidupan seharian. (Sebenarnya, julat ini jauh lebih luas.) Jelas sekali, ia tidak mencukupi untuk banyak peranti elektrik. Oleh itu, bateri jenis yang sama disambungkan secara bersiri, dan ini sering dilakukan dalam satu kes.
Contoh reka bentuk sedemikian ialah pembangunan automotif yang meluas berdasarkan asid sulfurik dan plat elektrod plumbum.
Biasanya, di kalangan orang, terutamanya di kalangan pemandu pengangkutan, adalah kebiasaan untuk memanggil mana-mana peranti bateri, tanpa mengira bilangan unsur konstituennya - kotak. Walau bagaimanapun, ini tidak sepenuhnya betul.Struktur, dipasang dari beberapa kotak yang disambungkan secara bersiri, sudah menjadi bateri, yang mana nama singkatan «АКБ» dilekatkan... Struktur dalamannya ditunjukkan dalam rajah.
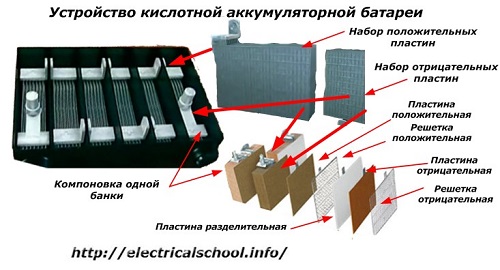
Setiap balang terdiri daripada dua blok dengan satu set plat untuk elektrod positif dan negatif. Blok sesuai antara satu sama lain tanpa sentuhan logam dengan kemungkinan sambungan galvanik yang boleh dipercayai melalui elektrolit.
Dalam kes ini, plat kenalan mempunyai grid tambahan dan dipisahkan antara satu sama lain oleh plat pemisah.
Menyambungkan plat dalam blok meningkatkan kawasan kerjanya, mengurangkan jumlah rintangan keseluruhan struktur dan membolehkan anda meningkatkan kuasa beban yang disambungkan.
Di bahagian luar kotak, bateri sedemikian mempunyai unsur-unsur yang ditunjukkan dalam rajah di bawah.
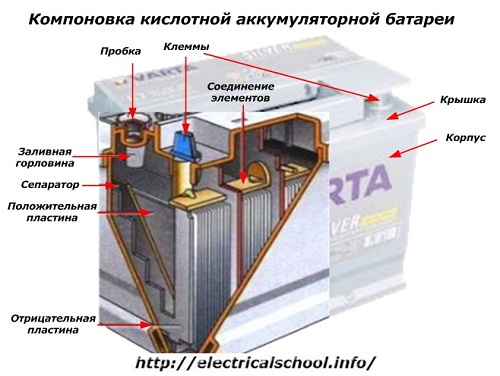
Ia menunjukkan bahawa perumahan plastik yang kukuh dimeterai dengan penutup dan dilengkapi dengan dua terminal (biasanya berbentuk kon) di atas untuk sambungan ke litar elektrik kereta. Tanda kekutuban dicap pada terminalnya: «+» dan «-«. Biasanya terminal positif mempunyai diameter lebih besar sedikit daripada terminal negatif untuk menyekat ralat pendawaian.
Bateri yang boleh diservis mempunyai lubang pengisi di bahagian atas setiap balang untuk mengawal paras elektrolit atau menambah air suling semasa operasi. Palam dipasang ke dalamnya, yang melindungi rongga dalaman kes daripada pencemaran dan pada masa yang sama menghalang elektrolit daripada tumpah apabila bateri dicondongkan.
Oleh kerana dengan cas yang kuat, gas daripada elektrolit adalah mungkin (dan proses ini mungkin semasa pemanduan intensif), lubang dibuat pada palam untuk mengelakkan tekanan di dalam kotak daripada meningkat.Oksigen dan hidrogen, serta wap elektrolit, keluar melalui mereka. Adalah disyorkan untuk mengelakkan situasi sedemikian yang melibatkan arus pengecasan yang berlebihan.
Angka yang sama menunjukkan sambungan unsur antara tebing dan susunan plat elektrod.
Bateri penghidup kereta (asid plumbum) berfungsi berdasarkan prinsip sulfasi berganda. Semasa pelepasan / pengecasan, proses elektrokimia berlaku pada mereka, disertai dengan perubahan dalam komposisi kimia jisim aktif elektrod dengan pelepasan / penyerapan air dalam elektrolit (asid sulfurik).
Ini menerangkan peningkatan dalam graviti tentu elektrolit semasa mengecas dan penurunan apabila bateri dinyahcas. Dengan kata lain, nilai ketumpatan membolehkan anda menilai keadaan elektrik bateri. Peranti khas digunakan untuk mengukurnya - hidrometer kereta.
Air suling, yang merupakan sebahagian daripada elektrolit bateri asid, bertukar menjadi keadaan pepejal - ais pada suhu negatif.Oleh itu, untuk mengelakkan bateri kereta daripada membeku dalam cuaca sejuk, perlu menggunakan langkah-langkah khas yang diperuntukkan dalam peraturan untuk eksploitasi.
Apakah jenis bateri yang ada?
Pengeluaran moden untuk pelbagai tujuan menghasilkan lebih daripada tiga dozen produk dengan komposisi elektrod dan elektrolit yang berbeza. 12 model yang diketahui dijalankan pada litium sahaja.

Yang berikut boleh didapati sebagai logam elektrod:
-
memimpin;
-
besi;
-
litium;
-
titanium;
-
kobalt;
-
kadmium;
-
nikel;
-
zink;
-
perak;
-
vanadium;
-
aluminium
-
beberapa barang lain.
Mereka menjejaskan ciri keluaran elektrik dan oleh itu aplikasinya.
Keupayaan untuk menahan beban tinggi jangka pendek yang terhasil daripada putaran aci engkol enjin pembakaran dalaman oleh motor pemula elektrik adalah ciri bateri asid plumbum. Ia digunakan secara meluas dalam pengangkutan, bekalan kuasa tidak terganggu dan sistem kuasa kecemasan.
Standard sel galvanik (bateri biasa) biasanya digantikan dengan bateri nikel-kadmium, nikel-zink dan nikel-logam hidrida.
Tetapi reka bentuk litium-ion atau litium-polimer berfungsi dengan pasti dalam peranti mudah alih dan pengkomputeran, alat pembinaan, dan juga kenderaan elektrik.
Mengikut jenis elektrolit yang digunakan, bateri adalah:
-
masam
-
beralkali.
Terdapat pengelasan bateri mengikut tujuan. Contohnya, dalam keadaan moden, peranti telah muncul yang digunakan untuk pemindahan tenaga — mengecas semula sumber lain. Bateri luaran yang dipanggil membantu pemilik banyak peranti mudah alih jika tiada rangkaian elektrik berselang-seli. Ia mampu mengecas berulang kali tablet, telefon pintar, telefon bimbit.
Semua bateri ini mempunyai prinsip operasi yang sama dan peranti yang serupa. Sebagai contoh, model jari litium-ion yang ditunjukkan dalam rajah di bawah dalam banyak cara mengulangi reka bentuk bateri asid yang dibincangkan sebelum ini.
Di sini kita melihat elektrod sentuhan yang sama, plat, pemisah dan perumah. Hanya mereka dibuat dengan mengambil kira keadaan kerja lain.
Ciri-ciri elektrik asas bateri
Operasi peranti dipengaruhi oleh parameter:
-
kapasiti;
-
ketumpatan tenaga;
-
pelepasan diri;
-
rejim suhu.
Kapasiti dipanggil cas maksimum bateri, yang ia mampu berikan semasa nyahcas ke voltan terendah. Ia dinyatakan dalam loket (sistem SI) dan jam ampere (unit bukan sistem).
Sebagai jenis kapasiti terdapat «kapasiti tenaga», yang menentukan tenaga yang dikeluarkan semasa nyahcas kepada voltan minimum yang dibenarkan. Ia diukur dalam joule (SI) dan watt-jam (unit bukan SI).
Ketumpatan tenaga dinyatakan sebagai nisbah jumlah tenaga kepada berat atau isipadu bateri.
Nyahcas sendiri pertimbangkan kehilangan kapasiti selepas mengecas jika tiada beban pada terminal. Ini bergantung kepada reka bentuk dan diburukkan lagi oleh kerosakan penebat antara elektrod atas pelbagai sebab.
Suhu operasi menjejaskan sifat elektrik dan sekiranya berlaku penyelewengan yang serius daripada norma yang ditentukan oleh pengilang, ia boleh merosakkan bateri. Haba dan sejuk tidak boleh diterima, ia menjejaskan perjalanan tindak balas kimia dan tekanan persekitaran di dalam kotak.
