Dielektrik kutub dan bukan kutub
Menurut pandangan fizik klasik, dielektrik pada asasnya berbeza daripada konduktor, kerana dalam keadaan biasa tidak ada cas elektrik percuma di dalamnya. Jumlah cas zarah yang membentuk molekul dielektrik adalah sifar. Walau bagaimanapun, ini tidak bermakna sama sekali bahawa molekul bahan ini tidak mampu mempamerkan sifat elektrik.
Semua dielektrik linear yang diketahui boleh dibahagikan kepada dua kumpulan besar: dielektrik kutub dan dielektrik nonpolar. Pembahagian ini diperkenalkan kerana perbezaan dalam mekanisme polarisasi molekul setiap jenis dielektrik. Malah, mekanisme polarisasi ternyata menjadi aspek yang sangat penting dalam kajian kedua-dua sifat fizikal dan kimia dielektrik, dan dalam kajian sifat elektriknya.
Dielektrik bukan kutub
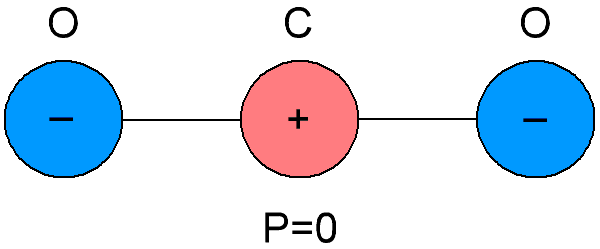
Dielektrik bukan kutub juga dipanggil dielektrik neutral, kerana molekul yang terdiri daripada dielektrik ini berbeza dalam kebetulan pusat graviti cas negatif dan positif di dalamnya.Akibatnya, ternyata molekul dielektrik bukan kutub tidak mempunyai momen elektrik sendiri, ia sama dengan sifar. Dan jika tiada medan elektrik luaran, cas positif dan negatif molekul bahan tersebut disusun secara simetri.
Jika medan elektrik luaran dikenakan pada dielektrik bukan kutub, maka cas positif dan negatif dalam molekul akan disesarkan daripada kedudukan keseimbangan asalnya, molekul akan menjadi dipol yang momen elektriknya kini akan berkadar dengan kekuatan elektrik. medan digunakan untuk mereka, dan akan diarahkan selari dengan medan.
Contoh dielektrik bukan kutub yang berjaya digunakan hari ini sebagai bahan penebat elektrik adalah seperti berikut: polietilena, polistirena, hidrokarbon, minyak penebat petroleum, dsb. Juga, wakil terang molekul bukan kutub adalah, sebagai contoh, nitrogen, karbon dioksida, metana, dll. Encik.
Dielektrik nonpolar, kerana nilai tangen kehilangan dielektriknya yang rendah, digunakan secara meluas sebagai dielektrik frekuensi tinggi dalam kapasitor seperti K78-2.
Dielektrik kutub
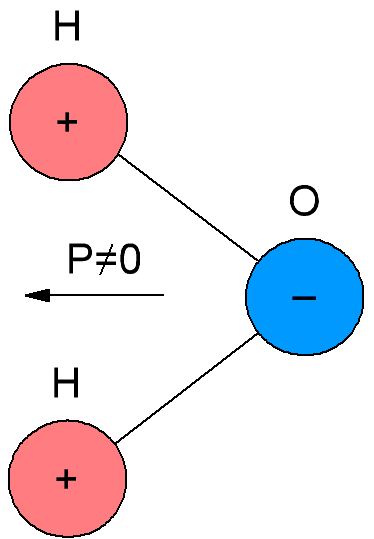
Dalam dielektrik kutub, yang juga dipanggil dielektrik dipol, molekul mempunyai momen elektrik mereka sendiri, iaitu, molekulnya adalah kutub. Sebabnya ialah molekul dielektrik kutub mempunyai struktur asimetri, jadi pusat jisim cas negatif dan positif dalam molekul dielektrik tersebut tidak bertepatan.
Jika dalam polimer bukan kutub beberapa atom hidrogen digantikan oleh atom unsur lain atau oleh radikal bukan hidrokarbon, maka kita hanya akan mendapat dielektrik polar (dipol), kerana simetri akan pecah akibat daripada penggantian. Menentukan kekutuban bahan dengan formula kimianya, penyelidik mesti, sudah tentu, mempunyai idea tentang struktur spatial molekulnya.
Apabila tiada medan elektrik luaran, paksi-paksi dipol molekul diorientasikan secara sewenang-wenangnya disebabkan oleh gerakan terma, supaya pada permukaan dielektrik dan dalam setiap unsur isipadunya cas elektrik adalah pada purata sifar. Walau bagaimanapun, apabila dielektrik dimasukkan ke dalam medan luaran, orientasi separa dipol molekul berlaku. Akibatnya, cas bersambung makroskopik yang tidak terkompensasi muncul pada permukaan dielektrik, mewujudkan medan yang diarahkan ke medan luaran.
Contoh dielektrik kutub termasuk yang berikut: hidrokarbon berklorin, resin epoksi dan fenol formaldehid, sebatian silikon silikon, dsb. Molekul air dan alkohol, sebagai contoh, juga merupakan contoh penting bagi molekul polar. Dielektrik kutub digunakan secara meluas dalam pelbagai bidang teknologi, seperti piezoelektrik dan feroelektrik, optik, optik tak linear, elektronik, akustik, dll.

